中国原研新一代肾素抑制剂首张处方落地 谱写高血压“源头降压”新篇章
2025年12月3日,上海医药研发的1类创新药苹果酸司妥吉仑片(以下简称司妥吉仑)获批上市,用于治疗原发性高血压。2026年2月10日,上海市浦东新区公利医院开出司妥吉仑全国首张处方,标志着我国高血压治疗领域正式迎来新一代口服非肽类小分子直接肾素抑制剂(DRI)。作为“源头降压”理念的创新实践,司妥吉仑为众多血压控制不佳或不耐受传统治疗方案的患者提供了全新的治疗选择。
司妥吉仑创新机制,开启高血压“源头治疗”新纪元
高血压是我国患病人数最多的慢性非传染性疾病。流行病学数据显示,自1958年以来,我国高血压患病率总体呈持续增高趋势。尽管患者对血压控制的意识不断加强,但我国高血压患者的知晓率、治疗率及控制率均有待提升,其中控制率仅为12.9%。这一现状意味着大量患者仍暴露于血压未达标所带来的心、脑、肾等靶器官损害风险之中,对于更有效、更安全且便于长期管理的降压药物存在巨大需求。
血压调控涉及复杂的病理生理机制,其中肾素-血管紧张素-醛固酮系统(RAAS)是核心系统。现有一线RAAS抑制剂,如血管紧张素转换酶抑制剂(ACEI)和血管紧张素II受体拮抗剂(ARB),虽广泛应用,但仍存在一定局限性。例如,ACEI可能导致咳嗽、血管性水肿等不良反应,而ARB则可能面临“肾素突破”现象,即蓄积的血管紧张素II与其他受体结合产生难以预测的生理效应。传统机制被比喻为“下游拦截”,由于切断了负反馈环路,会导致上游肾素活性(PRA)补偿性升高,产生“肾素逃逸”现象。
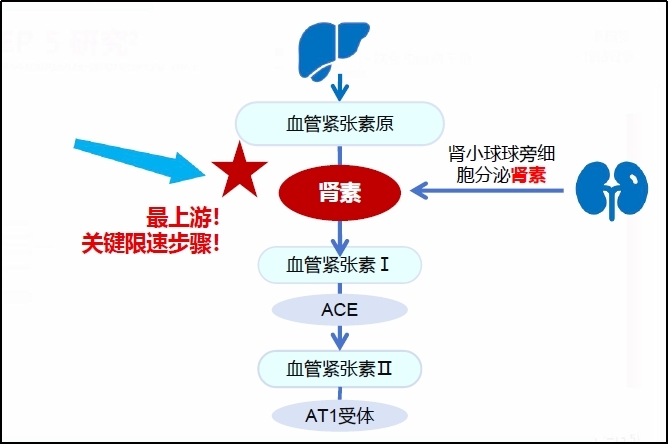
司妥吉仑与肾素结合抑制RAAS激活,直接抑制血管紧张素I和II的生成
司妥吉仑作为新一代口服非肽类小分子直接肾素抑制剂(DRI),其创新之处在于直击RAAS系统的“最上游”和“关键限速步骤”——肾素(图)。司妥吉仑通过直接抑制肾素活性,从源头阻止血管紧张素原转化为血管紧张素I,从而阻断后续血管紧张素II的生成以及醛固酮分泌、血管收缩等升压效应。这种“源头关小水龙头”的机制,能够显著降低PRA,实现源头阻断RAAS激活,避免了传统药物的“逃逸现象”。此外,司妥吉仑的分子量小,与肾素结合更紧密,通过形成多个氢键等相互作用实现强效抑制。因此,司妥吉仑不仅为血压控制提供了新路径,更在机制上区别于传统的“下游拦截”,为高血压治疗带来了“源头创新”的理念。
中国原研实证卓越,司妥吉仑奏响“安心”降压乐章
司妥吉仑的疗效与安全性得到了中国多项临床研究的充分验证。药效动力学研究显示,连续给药100 mg以上,服药0.5小时后血浆肾素活性即可得到迅速且明显的抑制,90%以上肾素活性抑制持续24小时,连续7天用药在人体无明显蓄积。
全国多中心、随机、双盲、双模拟、阳性药物平行对照的Ⅲ期临床试验(SPH3127-301研究),纳入828例原发性轻、中度高血压患者,随机分为缬沙坦组(n=415)和司妥吉仑组(n=413),观察治疗12周的疗效。随后222例患者在服用12周缬沙坦后转为服用司妥吉仑继续治疗40周,224例患者在服用12周司妥吉仑后继续服用司妥吉仑治疗40周。评价指标为各时间点的平均坐位舒张压(msDBP)和平均坐位收缩压(msSBP)相对基线的变化、各时间点的总有效率、达标率及安全性指标。
研究结果显示,司妥吉仑的降压疗效与安全性均表现突出。研究证实,每日一次口服100 mg司妥吉仑,连续用药12周,可安全、有效地降低原发性高血压患者的血压,为主要疗效指标msDBP的下降提供了确凿证据,不仅降压效果明确,且能实现长期稳定控压。治疗52周时,维持司妥吉仑方案的患者血压下降显著,同时治疗总有效率和达标率也呈现进一步提高的趋势。此外,司妥吉仑为口服给药,每日一次口服100 mg,用药方便,患者的依从性较好。
《中国高血压防治指南(2024年修订版)》明确指出,直接肾素抑制剂作用机制在于直接抑制肾素,继而减少血管紧张素Ⅱ的产生,可显著降低高血压患者的血压水平。这为司妥吉仑在临床实践中的使用提供了明确的循证依据。司妥吉仑首张处方的落地,其意义超越了在心血管治疗领域增加一个新的降压药选项,它标志着“直接肾素抑制”这一创新治疗策略在中国正式进入临床实践,是中国原研力量在高血压治疗源头创新上的重要突破。随着其临床应用经验的不断积累,司妥吉仑有望为优化我国高血压管理格局、提升整体控制水平贡献重要价值。